干細(xì)胞 生命科學(xué)的“萬(wàn)能鑰匙”在癌癥、糖尿病與組織修復(fù)中的革命性突破

在生命科學(xué)飛速發(fā)展的今天,干細(xì)胞技術(shù)以其非凡的再生與修復(fù)潛力,被譽(yù)為“萬(wàn)能細(xì)胞”或生命科學(xué)的“萬(wàn)能鑰匙”。它在癌癥治療、糖尿病管理以及組織修復(fù)等重大醫(yī)學(xué)挑戰(zhàn)面前,正展現(xiàn)出前所未有的價(jià)值,引領(lǐng)著一場(chǎng)深刻的醫(yī)療革命。
一、 攻克癌癥堡壘:從精準(zhǔn)靶向到免疫重塑
傳統(tǒng)癌癥療法如化療和放療,在殺傷癌細(xì)胞的往往“傷敵一千,自損八百”,對(duì)正常細(xì)胞造成嚴(yán)重?fù)p害。干細(xì)胞技術(shù)為癌癥治療開辟了新維度:
- CAR-T細(xì)胞療法:這是目前最成功的干細(xì)胞衍生療法之一。通過(guò)基因工程改造患者自身的T細(xì)胞(一種免疫細(xì)胞),使其表達(dá)能特異性識(shí)別癌細(xì)胞的嵌合抗原受體(CAR),再回輸?shù)交颊唧w內(nèi),形成一支精準(zhǔn)的“抗癌大軍”。該療法已在某些血液腫瘤(如白血病、淋巴瘤)中取得驚人療效。
- 間充質(zhì)干細(xì)胞(MSCs)的輔助治療:MSCs具有強(qiáng)大的免疫調(diào)節(jié)和抗炎特性。在癌癥治療中,它們可用于:
- 緩解治療副作用:修復(fù)因放化療受損的腸道黏膜、減輕移植物抗宿主病(GVHD)。
- 作為藥物遞送載體:利用其腫瘤歸巢能力,攜帶抗癌藥物直達(dá)腫瘤部位,提高療效并降低全身毒性。
- 疾病建模與藥物篩選:利用誘導(dǎo)多能干細(xì)胞(iPSC)技術(shù),將患者體細(xì)胞重編程為干細(xì)胞,再分化為特定細(xì)胞(如肝細(xì)胞、肺細(xì)胞),用于構(gòu)建疾病模型,篩選個(gè)性化抗癌藥物。
二、 應(yīng)對(duì)糖尿病挑戰(zhàn):重建胰島素生產(chǎn)的希望
糖尿病,特別是1型糖尿病,源于胰島β細(xì)胞被自身免疫系統(tǒng)破壞,導(dǎo)致胰島素絕對(duì)缺乏。干細(xì)胞技術(shù)旨在從根本上解決這一問題:
- β細(xì)胞替代療法:科研人員已成功將胚胎干細(xì)胞(ESC)或iPSC分化為能夠分泌胰島素的β樣細(xì)胞。將這些細(xì)胞移植到患者體內(nèi),有望替代受損的胰島細(xì)胞,恢復(fù)生理性的血糖調(diào)節(jié)。這是最具前景的“治愈性”研究方向之一。
- 免疫調(diào)節(jié)治療:利用間充質(zhì)干細(xì)胞(MSCs)調(diào)節(jié)紊亂的自身免疫系統(tǒng),保護(hù)殘存的β細(xì)胞功能,延緩疾病進(jìn)程,為2型糖尿病的炎癥控制也提供了新思路。
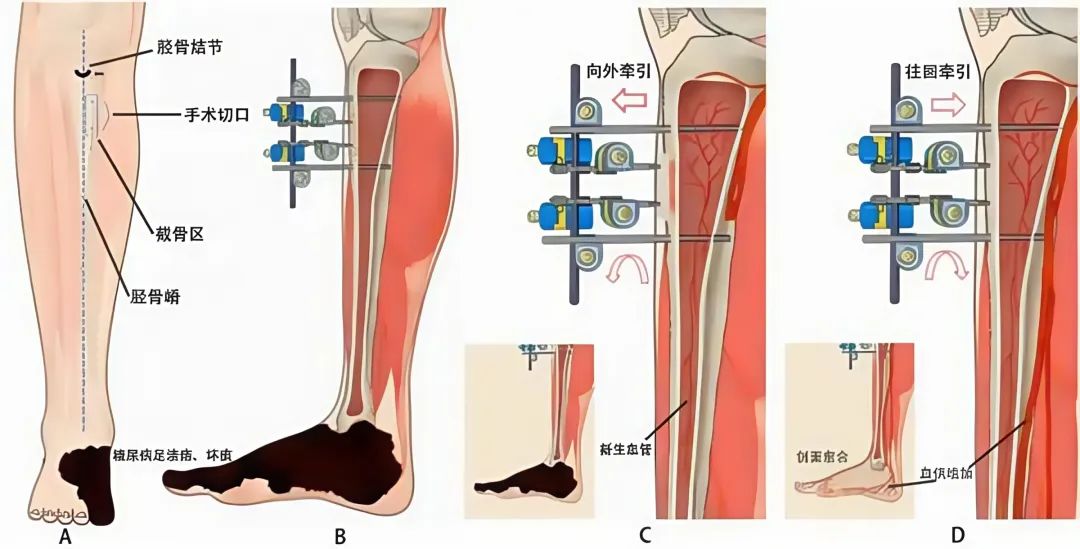
- 血管與神經(jīng)并發(fā)癥修復(fù):糖尿病常伴隨下肢缺血、糖尿病足、神經(jīng)病變等嚴(yán)重并發(fā)癥。MSCs通過(guò)促進(jìn)血管新生、調(diào)節(jié)炎癥、分泌營(yíng)養(yǎng)因子,在促進(jìn)潰瘍愈合、修復(fù)神經(jīng)損傷方面展現(xiàn)出治療潛力。
三、 實(shí)現(xiàn)組織修復(fù)與再生:從概念走向臨床
干細(xì)胞的核心能力在于其多向分化和自我更新潛能,使其成為組織修復(fù)的理想“種子細(xì)胞”。
- 骨與軟骨修復(fù):利用MSCs或脂肪干細(xì)胞結(jié)合生物支架材料,修復(fù)骨缺損、骨關(guān)節(jié)炎軟骨損傷,避免了傳統(tǒng)手術(shù)的創(chuàng)傷和人工關(guān)節(jié)的局限。
- 心臟修復(fù):心肌梗死會(huì)導(dǎo)致心肌細(xì)胞大量死亡,形成不可逆的疤痕。干細(xì)胞移植(如心臟干細(xì)胞、MSCs)旨在促進(jìn)心肌再生、改善心臟功能、減少疤痕形成,為心力衰竭患者帶來(lái)新希望。
- 神經(jīng)系統(tǒng)修復(fù):針對(duì)帕金森病、脊髓損傷、腦卒中等,干細(xì)胞(如神經(jīng)干細(xì)胞、MSCs)移植可替代受損的神經(jīng)元或神經(jīng)膠質(zhì)細(xì)胞,分泌神經(jīng)營(yíng)養(yǎng)因子,為神經(jīng)再生創(chuàng)造微環(huán)境。
- 皮膚與角膜再生:干細(xì)胞技術(shù)已成功應(yīng)用于嚴(yán)重?zé)齻钠つw再生、角膜損傷修復(fù),大大改善了患者的生活質(zhì)量。
人體干細(xì)胞技術(shù)開發(fā)與應(yīng)用的挑戰(zhàn)與未來(lái)
盡管前景廣闊,干細(xì)胞技術(shù)的全面應(yīng)用仍面臨諸多挑戰(zhàn):
- 安全性:包括致瘤風(fēng)險(xiǎn)、免疫排斥、異常分化等。
- 有效性:如何確保移植細(xì)胞在體內(nèi)的長(zhǎng)期存活、穩(wěn)定功能和高效整合。
- 標(biāo)準(zhǔn)化與規(guī)模化:細(xì)胞制備、質(zhì)量控制和治療方案的標(biāo)準(zhǔn)化是臨床推廣的關(guān)鍵。
- 倫理與法規(guī):特別是涉及胚胎干細(xì)胞的研究,需在嚴(yán)格的倫理框架和監(jiān)管政策下進(jìn)行。
隨著基因編輯技術(shù)(如CRISPR)、3D生物打印、類器官技術(shù)與干細(xì)胞研究的深度融合,個(gè)性化、精準(zhǔn)化的“定制”細(xì)胞治療將成為可能。從實(shí)驗(yàn)室研究到臨床轉(zhuǎn)化,從治療罕見病到應(yīng)對(duì)常見慢性病,干細(xì)胞技術(shù)正穩(wěn)步推動(dòng)醫(yī)學(xué)進(jìn)入一個(gè)“再生修復(fù)”的新時(shí)代。它不僅是對(duì)抗疾病的利器,更是人類理解生命、重塑健康的全新篇章。
如若轉(zhuǎn)載,請(qǐng)注明出處:http://www.no1yy.com.cn/product/60.html
更新時(shí)間:2026-04-12 21:01:23